6. Calixarène : (6.7) - Corrigé
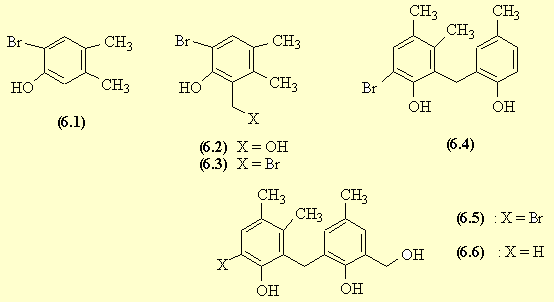
- La première étape de la synthèse est une SE sur le noyau aromatique. Le groupe OH est le groupe orienteur la position para est bloquée et l'une des positions ortho est moins encombrée que l'autre : c'est là que le brome se placera majoritairement dans (6.1). La SE du formaldéhyde sur le noyau aromatique (en milieu basique pour augmenter la nucléophilie du noyau aromatique du phénol) permet l'introduction d'un groupement hydroxyméthyle sur la position ortho qui reste vacante.
- Une SN par HBr permet la transformation de la fonction alcool en bromure (6.3). Cet halogènure benzylique donne facilement un carbocation.
- (6.4) résulte d'une nouvelle SE de ce carbocation benzylique sur le p-crésol. L'élimination de l'atome de brome libère une position en ortho de la fonction phénol. En milieu acide, la fonction alcool benzylique donne un nouveau carbocation qui réagit sur la position ortho libérée d'une deuxième molécule. Les deux réactions identiques conduisent au cycle du calixarène (6.7).
- L'introduction du brome dans la première étape sert à bloquer cette position pour éviter l'introduction d'une seconde molécule de formaldéhyde dans le passage de (6.1) à (6.2) et une autocondensation lors du passage de (6.3) à (6.4).