11. Pridéfine : (11.3) - Correction
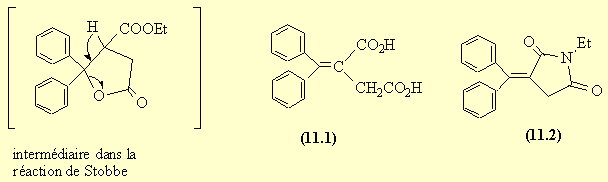
- La première étape de cette synthèse est une réaction de Stobbe qui débute par l'addition du carbanion du succinate sur la benzophénone (AdN). La lactone intermédiaire donne une réaction d'élimination. La fonction ester restante est saponifiée. L'acidification conduit au diacide (11.1) qui, dans les conditions opératoires utilisées, ne donne pas de décarboxylation.
- L' imide (11.2) est obtenu par réaction de ce diacide avec l'amine primaire.
- La réduction de cet imide comme celle d'un amide conduit à l'amine(11.3).
- Le produit (11.1) contient deux fonctions acides. L'une est une fonction acide a,b- éthylénique qui serait donc moins réactive (effet +M donneur de la double liaison).