9. Ciramadol : (9.4) - Corrigé
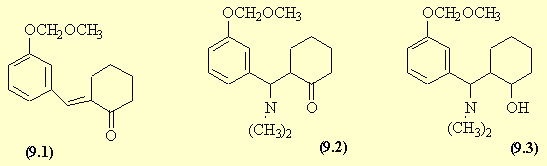
- La première réaction est une aldolisation croisée (c'est la cyclohexanone qui donne le carbanion) ; cette réaction est suivie d'une déshydratation qui se fait facilement car la double liaison formée est conjuguée avec la fonction carbonyle et le cycle aromatique.
- La deuxième réaction est une addition de Michael sur la cétone α,β- éthylénique (AdN).
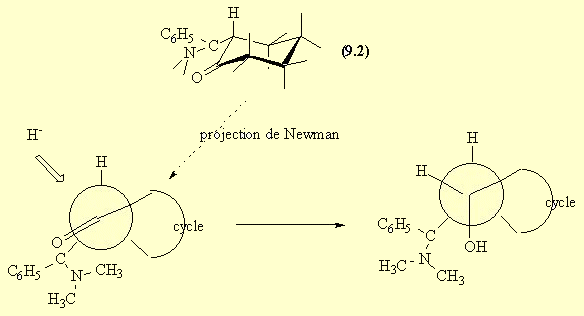
- La troisième réaction est une réduction (ou AdN d'un ion H-). Enfin la dernière étape est une hydrolyse de l'acétal. Dans cette dernière étape on récupère le phénol (9.4) mais aussi le méthanol et le formaldéhyde.
- L'entrée majoritaire de l'ion H- du côté le moins encombré dans (9.2), conduit bien au cis amino alcool.