- Synthèse recherche

- Les quatre premières réactions sont des substitutions nucléophiles, probablement de type SN2 à partir successivement : d'un phénate, d'une amine primaire, d'une amine secondaire et d'un phénate.
- Une hydrogènolyse redonne une amine secondaire (et du toluène !).
- Une résolution permet d'isoler l'énantiomère qui conduira au produit "actif".
- Enfin une SN sur la fonction ester donne l'amide final
(34.6).
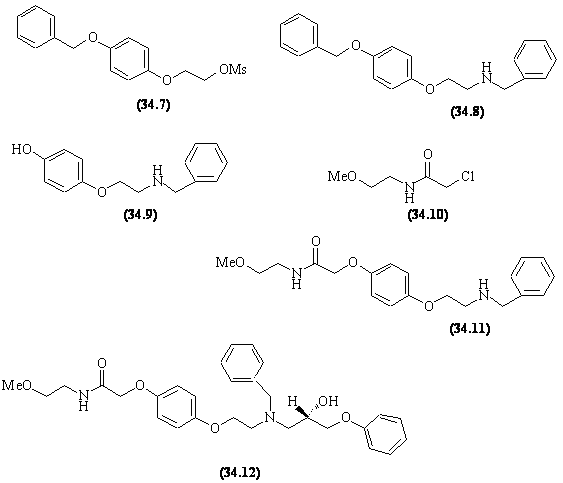
- Synthèse production
- Deux substitutions nucléophiles débutent cette séquence.
- Une hydrogènolyse chimiosélective de l'éther benzylique permet de retrouver une fonction phénol (et du toluène), précédemment " bloquée".
- Dans le chlorure de chloroacétyle, la fonction chlorure d'acide est plus réactive vis à vis de la SN que la fonction chlorure d'alkyle et on obtient (34.10).
- La SN du phénate formé à partir de (34.9), sur le chloro-amide donne (34.11).
- Une SN2 régiosélective de l'amine secondaire sur l'époxyde de configuration S conduit à (34.12) dans lequel la configuration du carbone est conservée.
- Enfin une hydrogènolyse de cette amine benzylique redonne la fonction amine secondaire.
Dans les deux première étapes, les SN sur les sulfonates libèrent des produits secondaires à évacuer : dans ce cas, de l'acide méthanesulfonique (sous forme de sel de sodium) ou de l'acide toluène sulfonique si on avait utilisé un bis-tosylate. A nombre de moles égal, l'acide méthanesulfonique représente en masse moins de produit donc nécessite un matériel (filtres, conteneurs etc....) moins volumineux, ce qui est un avantage important au stade industriel.