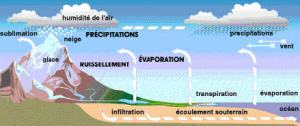
L'eau milieu naturel
Constituant essentiel de la matière vivante (>70% du corps humain, >90% des plantes).
1. Différents types d'eau
|
2. Potabilité de l'eau
les critères : goût, stérilité, aspect, salinité (dureté)
Titre Hydrotimétrique (dureté de l'eau) en °TH : $\text{1 }\!\!{}^\circ\!\!\text{ TH = 10mg}\text{.}{{\text{l}}^{\text{-1}}}\text{CaC}{{\text{O}}_{\text{3}}}$
Sels fréquents :
$\text{CO}_{\text{3}}^{\text{2-}}$, $\text{H}CO_{3}^{-}$, $SO_{4}^{2-}$, $\text{C}{{\text{l}}^{-}}$ , $\text{NO}_{3}^{-}$
$C{{a}^{2+}}$, $M{{g}^{2+}}$, $\text{N}{{\text{a}}^{+}}$, ${{\text{K}}^{+}}$, $\text{F}{{\text{e}}^{3+}}$,
attention aux anions oxydants comme les nitrates provenant des activités agricoles et des élevages intensifs.
Stérilisation par oxydation avec $\text{C}{{\text{l}}_{\text{2}}}$ ou $\text{NaOCl}$ (goût d'eau de javel), ozone ou par irradiation UV
Goût, aspect importance de la décantation et de la filtration.
3. L'eau et la corrosion
Dépôts calcaire :
Calcaire $\text{CaC}{{\text{O}}_{\text{3}}}$ déposé par décomposition de l'hydrogénocarbonate de calcium $\text{Ca(HC}{{\text{O}}_{\text{3}}}{{\text{)}}_{\text{2}}}$ , (dissolution par des solutions acides faibles comme l'acide acétique ou l'acide citrique).
Voir le cours sur la précipitation et la solubilité des sels dans le module "Chimie en solution".
tartre $\text{CaS}{{\text{O}}_{\text{4}}}$ (très dur et isolant thermique formé dans les circuits de chauffage, difficile à décomposer).
Corrosion métallique : un métal M est corrodé dès que sa concentration dissous dans l'eau dépasse ${{10}^{-6}}mole.{{l}^{-1}}$
Par exemple, dans le cas de la formation de la rouille, les équilibres qui conduisent à la corrosion du fer sont les suivants:
Le fer est oxydé en milieu acide par ${{\text{H}}^{\text{+}}}$ : $Fe+2{{H}^{+}}\to F{{e}^{2+}}+{{H}_{2}}$
Puis l'oxygène dissous dans l'eau oxyde le fer (+II) en fer (+III) : $4F{{e}^{2+}}+{{O}_{2}}+2{{H}_{2}}O\to \text{ }4Fe{{\left( OH \right)}_{3}}$
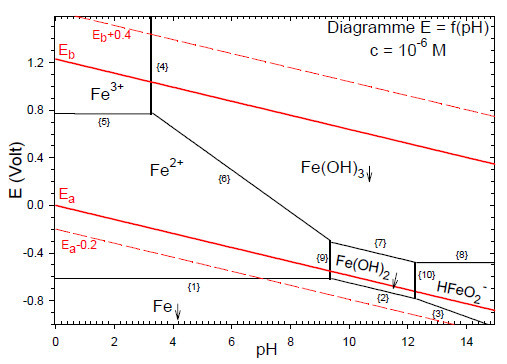
Le diagramme de corrosion du fer ( $c={{10}^{-6}}M$ ) montre ainsi que le fer se corrode à l'air en milieu humide si : $4\le pH\le 12$.
La corrosion cesse si le résultat est adhérent et oxydé, c'est pour cela que l'on réalise des oxydations chimiques par phosphatation ou par chromatation .