Equilibre liquide-solide - (binaires)
Mode de représentation à P=Cste : $v=n+1-\varphi =3-\varphi $. On trace T = f(composition) en % molaire (ou % atomique).
La courbe de liquidus est la courbe au-dessus de laquelle n'existe que du liquide.
La courbe de solidus est la courbe au-dessous de laquelle n'existe que du solide.
v=0 (point invariant) $\varphi =3$ Transformation isotherme, domaine triphasé
Exemples :
liquide $\to $ solide (1) + solide (2) c'est le cas de l'eutectique
solide (3) $\to $ solide (1) + solide (2) c'est le cas de l'eutectoïde
v=1 (on fixe T) $\varphi =2$ Domaine biphasé
v=2 (on fixe T et la composition) $\varphi =1$ Domaine monophasé
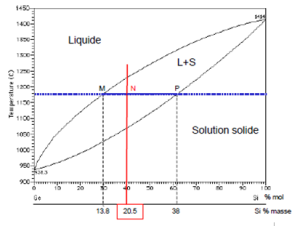
Règle des moments chimiques (ou des leviers). Dans un domaine biphasé, il est intéressant de connaître la proportion des phases en présence dans le mélange pour une température donnée. A la température T, le mélange de composition X (point N) est constitué des phases ${{\phi }_{1}}$ ( liquide) et ${{\phi }_{2}}$ (solide) :
|
$$\begin{align}& \text{ }{{m}_{1}}\frac{{{X}_{1}}}{100}+{{m}_{2}}\frac{{{X}_{2}}}{100}=m\frac{X}{100} \\& {{m}_{1}}{{X}_{1}}+{{m}_{2}}{{X}_{2}}=mX=({{m}_{1}}+{{m}_{2}})X \\& \text{ }{{m}_{1}}(X-{{X}_{1}})={{m}_{2}}({{X}_{2}}-X) \\\end{align}$$
Alors : ${{m}_{1}}.NM\text{ }=\text{ }{{m}_{2}}.NP$
Exemple :
A 1180°C, 100g d'un mélange de Ge-Si à 20,5% en masse de silicium est constitué du mélange d'un solide et d'un liquide tel que :
$$\frac{{{m}_{1}}}{{{m}_{2}}}=\frac{NP}{NM}=\frac{38-20.5}{20.5+13.8}=2.612\text{ si }m={{m}_{1}}+{{m}_{2}}=100g$$
Alors : ${{m}_{2}}=\frac{{{m}_{1}}}{2.612}=\frac{m-{{m}_{2}}}{2.612}\text{ et }{{m}_{2}}.(2.612+1)=m=100$
${{m}_{2}}=\frac{m}{3.612}=27.8\text{ }g$ de solide de composition à 38% massique en Si
${{m}_{1}}=72.2\text{ }g$ de liquide de composition à 13.8% massique en Si