
| |
 |
|
La structure cristalline des solides inorganiques
Les notions fondamentales - Les empilements de sphčres
1. Pourquoi étudier les solides ?
2. Quelques notions de base sur la périodicité
3. Représentation des structures
4. Empilement compact de sphčres
6. Les sites intersticiels dans les empilements compacts
Pourquoi étudier les solides ?
1. Tous les composés sont solides sous certaines conditions de température et de pression..
Certains n'existent qu'ŕ l'état solide
2. Les solides ont une trčs grande importance technologiquePropriétés mécaniques
Propriétés électriques
Propriétés magnétiques
Propriétés optiques
Catalyseurs
Senseurs
3. Les solides (surtout les monocristaux) ont toujours fasciné.
Quelques repčres historiques
(X-date = depuis la découverte de la diffraction
des rayons X - 1912) - BX = avant - AX = Aprčs -)
|
Date |
X-Date |
Evčnement |
|
ca. 6000 BC |
|
Les égyptiens extraient la turquoise |
|
Antiquité |
|
Les gemmes (particuličrement diamant, saphir, émeraude & rubis) sont trčs appréciés |
|
400 BC |
ca. 2310 BX |
Théophraste décrit la forme réguličre des cristaux de grenats |
|
64 BC |
1976 BX |
Strabo nomme Quartz krystlloz (crystallum en Latin), en fait notre 'cristal' |
|
1597 |
315 BX |
L'alchimiste Libavius constate que la forme géométrique des cristaux est caractéristique des sels concernés. |
|
17čme S |
ca. 302 BX |
Boyle, Leeuwenhoek, Kepler, Hooke... font de nombreuses observations avec le microscope récemment inventé |
|
1611 |
301 BX |
Kepler suggčre que la symétrie hexagonale des flocons de neige est due ŕ un empilement régulier des particules les constituant" |
|
1665 |
247 BX |
Hooke suggčre que les cristaux sont composés de "spheroďdes" |
|
1669 |
243 BX |
Steno observe que les cristaux de Quartz ,quelle que soit leur origine montrent les męmes angles interfaciaux caractéristiques. |
|
1780 |
132 BX |
Carangeot invente le Goniomčtre par contact- il mesure les angles interfaciaux permettant d'accéder ŕ un grand nombre de données cristallographiques. |
|
1783 |
129 BX |
Les études de Bergman sur le clivage des cristaux (sans doute de la calcite) lui suggčre que le cristal est formé d'unités rhombočdriques empilées. |
|
1783 |
129 BX |
de l'Isle formule la loi de constance des angles entre les faces. |
|
1801 |
111 BX |
Haüy introduit la loi des 'indices rationnels' Les lois fondamentales de la morphologie cristalline sont établies. |
|
1808 |
104 BX |
Malus constate la polarisation de la lumičre par certains cristaux |
|
1809 |
103 BX |
Wollaston invente le goniomčtre par réflexion. Ceci conduit ŕ une trčs grande amélioration de la précision sur les données angulaires. |
|
1815 |
97 BX |
Biot découvre les formes levo- et dextro-gyres du Quartz |
|
1819-22 |
93 BX |
Mitscherlich découvre : l'Isomorphisme (des cristals de différentes compositions peuvent avoir la męme forme) le Polymorphisme (des cristaux de formes différentes peuvent avoir la męme composition) [= Allotropie] |
|
1839 |
73 BX |
Miller utilise les Indices de Miller pour désigner les faces du cristal |
|
1848 |
64 BX |
Pasteur découvre les cristaux énantiomorphes |
|
1880s-90s |
32 BX |
Sohncke, Federov, Schönfleiß & Barlow développent la théorie de la symétrie interne cristalline - mais ne dispose pas de faits expérimentaux pour valider leurs théories |
|
1906-19 |
6 BX |
"Chemische Krystallographie" de Groth tabule les propriétés morphologiques, optiques et autres de 7000 substances cristallisées (pas d'information sur la structure interne - pas de techniques expérimentales). |
|
1907 |
5 BX |
Barlow & Pop proposent que dans un cristal les ions se comportent comme des sphčres dures en contact. |
|
1912 |
|
Friedrich, Knipping & von Laue découvrent la diffraction des rayons X |
|
1913 |
1 AX |
W.H. & W.L. Bragg utilisent la dépendance en orientation de la diffraction des rayons X d'un monocristal pour résoudre la structure de NaCl (& ensuite diamant etc...) |
|
1913 |
1 AX |
Ewald introduit le concept du Réseau Réciproque |
|
1914 |
2 AX |
Théorie de Debye de l'agitation thermique des atomes dans un solide (et donc le facteur Debye-Waller dans les structures cristallines ) |
|
1916 |
4 AX |
Expériences de Debye & Scherrer de diffraction des poudres |
|
1924 |
12 AX |
Bernal et al. - structure du Graphite |
|
1926 |
14 AX |
Défauts de structures étudiés par Frenkel |
|
1926 |
14 AX |
Formulation de l'atome sphérique par Goldschmidt |
|
1927 |
15 AX |
Reprise du Model ionique de Goldschmidt par Pauling dans les rčgles de Pauling |
|
1929 |
17 AX |
Générateur de rayons X ŕ anode tournante - autorise des intensités du rayonnement X plus fortes pour de meilleurs clichgés de diffraction. |
|
1934 |
22 AX |
Fonction de Patterson pour résoudre la structure par diffraction des rayons X |
|
1934 |
22 AX |
Ruska prend des images avec le premier microscope électronique ŕ transmission. |
|
1936 |
24 AX |
Halaban & Preiswerk -diffraction des neutrons par un cristal |
|
1941 |
29 AX |
Hughes utilise l'affinement par moindres-carrés pour obtenir le meilleur résultat possible ŕ partir d'un jeu de données de diffraction. |
|
1944 |
32 AX |
Buerger invente la chambre de précession |
|
1948 |
36 AX |
Harker & Kasper - Méthodes directes pour la résolution de la structure ŕ partir de données de diffraction X. |
|
1950s |
ca. 38 AX |
Les diffractomčtres automatiques et les ordinateurs facilitent considérablement la détermination des structures cristallines. |
|
1951 |
39 AX |
Bijvoet utilise la diffusion anomale pour déterminer la chiralité (configuration absolue) |
|
mi - 1950 |
ca. 43 AX |
Premičres utilisations des ordinateurs pour résoudre des structures cristallines. |
|
1955 |
43 AX |
Principes de Laves - remplissage de l'espace dans les cristaux |
|
1956 |
44 AX |
Menter obtient la premičre image d'un réseau par microscopie électronique ŕ transmission (TEM). |
|
1957 |
45 AX |
Müller - La microscopie d'émission de champ permet de visualiser des atomes dans un métal. |
|
1970 |
58 AX |
Crewe, Wall et Langmore - Microscopie électronique ŕ balyage en champ sombre (premičre méthode pour imager les atomes lourds individuellement) |
|
1971 |
59 AX |
Formanek et al. - Premičre détection d'un atome isolé en microscopie électronique ŕ transmission ŕ haute résolution(HREM) |
|
1974 |
62 AX |
Iijima - premičre observation de défauts ponctuels dans des structures par microscopie électronique |
|
1980s |
ca. 68 AX |
Rayonnement Synchrotron disponible - augmentation énorme de l'intensité des rayons X (clichés de Laue obtenus en quelques ms) |
|
1982 |
70 AX |
Détecteurs de rayons X bidimensionnels (gain de temps important pour la réalisation des clichés de diffraction X) |
|
1982 |
70 AX |
Binnig & Rohrer - Microscope ŕ balayage ŕ effet tunnel (STM) permet d'imager aussi les atomes légers en surface |
|
1984 |
72 AX |
Schechtman et al. découvrent les quasi-cristaux |
|
198? |
7? AX |
Binnig et al. - La Microscopie ŕ force atomique (AFM) permet d'obtenir des images des surfaces (souvent plus pratique que le STM) |
|
1990 |
ca. 80 AX |
Les données (coordonnées internes) de >200,000 structures cristallines sont enregistrées dans des bases de données. |
Quelques notions de base sur la périodicité
RESEAU = Un ensemble infini de noeud (points) dans l'espace, chaque noeud (point) a le męme environnement que ses voisins.
STRUCTURE CRISTALLINE = L'arrangement périodique des atomes dans le cristal. Il peut ętre décrit en associant ŕ chaque noeud du réseau un groupe d'atomes appelé le MOTIF.
MAILLE = C'est le plus petit
élément du cristal qui, répété par des translations successives reproduit le
cristal entier.
|
|
 |
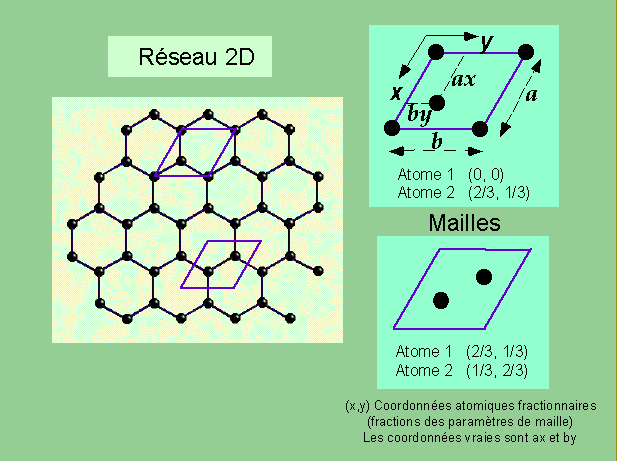
RESEAUX 2D :
Exemple d'une couche dans la structure du GRAPHITE
| Décompte des noeuds et des atomes
|
 |
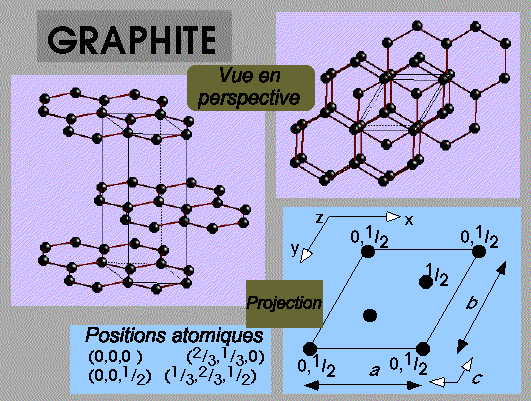
Etude d'un solide 3D : le Graphite
C'est un arrangement en zigzag de couches hexagonales
Décompte des atomes
® 1/8 atome par maille ® 1/4 atome par maille ® 1/2 atome par maille ® 1 atome par maille |
 |
Les 14 réseaux de BRAVAIS
La combinaison des 7 systčmes cristallins avec les modes de réseaux possibles conduit aux 14 réseaux 3D de Bravais

La combinaison de tous les éléments de symétrie dans les 14 réseaux de Bravais &emdash;> 230 groupes spatiaux

Empilement compact de sphčres
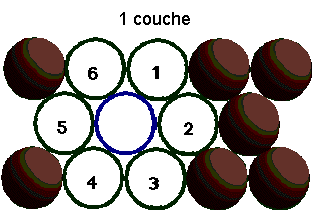
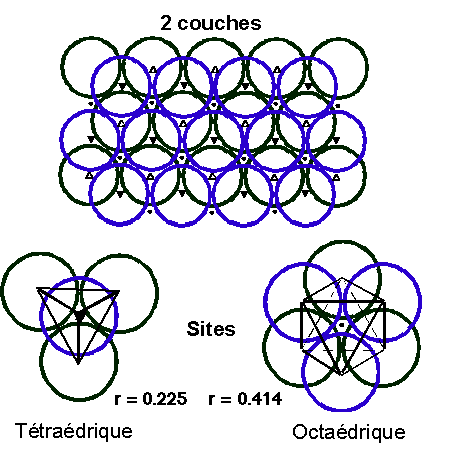
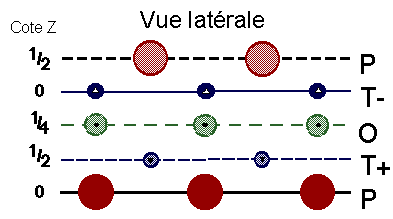



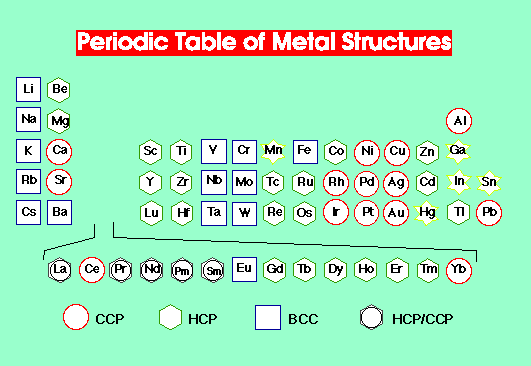
Les structures compactes les plus connues sont celles des métaux
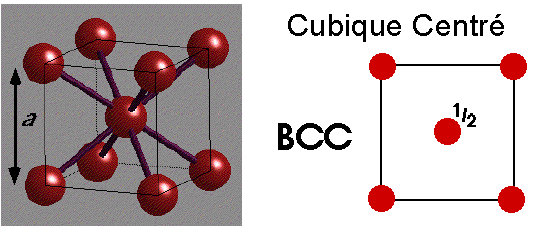
Une structure semi-compacte adoptée par certains métaux
|
68% de l'espace est occupé Nombre de coordination ?
|
 |
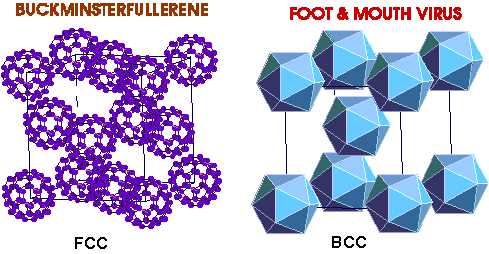
Les sites intersticiels dans les empilements compacts
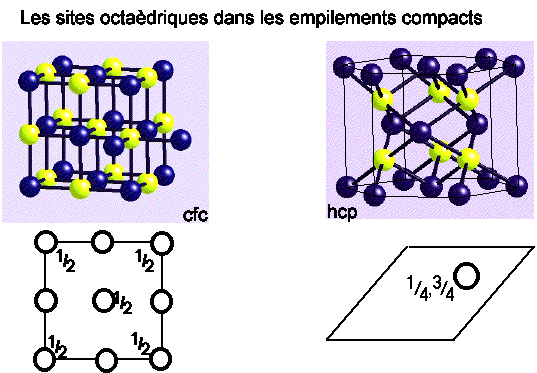
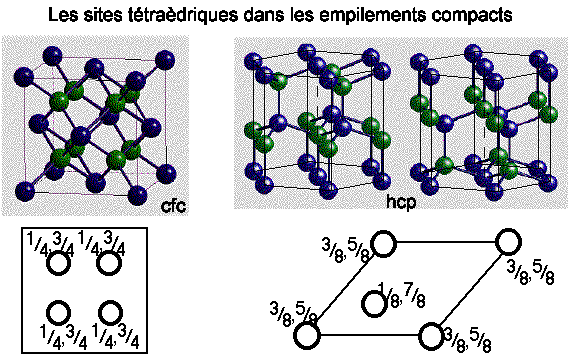
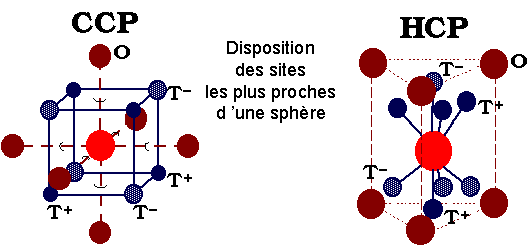

| |
Lecture 2 - Lecture 3 - Lecture 4 |
|
© S.J.Heyes , Oxford, 1996 Traduction -Adaptation : C. Jacoboni, Le Mans, 1998
Dernière mise à jour : 14/07/02