| |
 |
|
| |
 |
|
Structures des Solides simples inorganiques
(4) par Dr
S.J. Heyes
Traduction et adaptation :
Pr C. Jacoboni - Université du Maine
|
|
|
|
|
|
2. Connectivité - Approche topologique des structures
|
|
|
|
|
|
|
Cristobalite (SiO2) / Cuprite (Cu2O) |
|
|
|
|
STRUCTURES DES OXYDES METALLIQUES
Les oxydes métalliques sont parmi les plus importants des solides inorganiquesRutile, TiO2
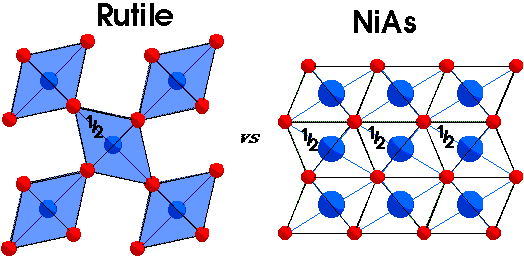
i.e. le rutile est un arrangement hcp distordu d'oxygčne avec les Ti dans la moitié des sites octaédriques
Trioxyde de Rhenium, ReO3
Perovskite, CaTiO3
|
1 CaTiO3 par maille Ca ŕ (1/2, 1/2, 1/2); 3 O ŕ (1/2, 0, 0), (0, 1/2, 0), (0, 0, 1/2) Ti 6 par O (octačdre) O octačdre distordu (4xCa + 2xTi) Cubocatčdres CaO12 liés par les faces |
|
|
La structure pérovskite est complčtement prévue par la 2éme rčgle de Pauling |
|
La2CuO4 {Structure type K2NiF4}
| La2-xSrxCuO4 dopé fut le premier oxyde supraconducteur ŕ haute Température critique (1986) (Tc ~ 40 K) | |
| La2CuO4 peut
ętre vu comme construit ŕ partir d'un arrangement ABAB... de mailles pérovskites
|
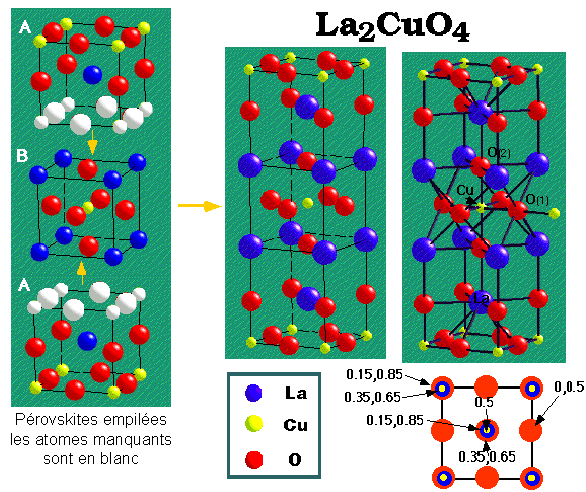 |
Différentes vues de la structure La2CuO4
On peut voir la structure comme
basée sur :
|
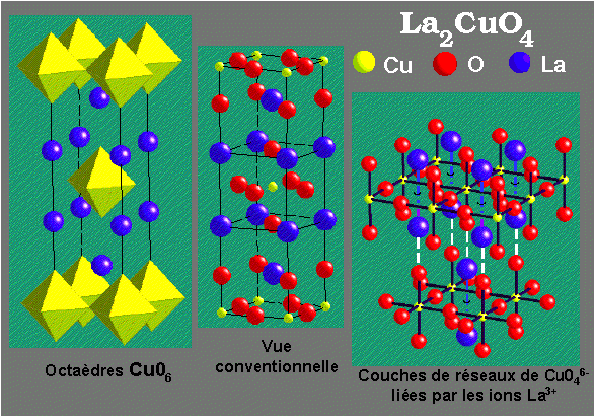 |
Comparaison des structures La2CuO4 et Nd2CuO4
|
|
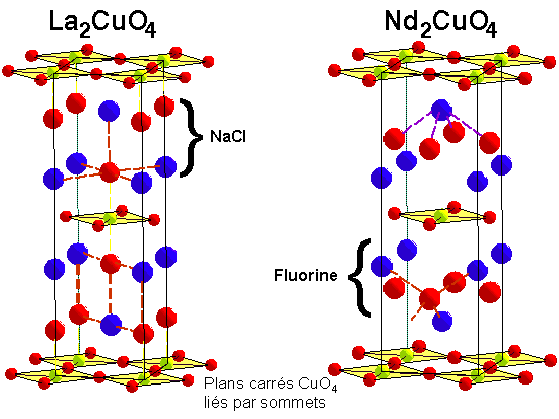 |
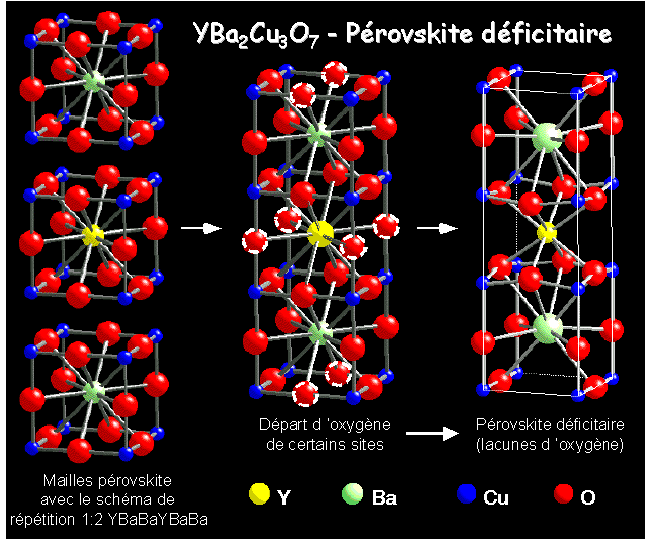
| YBa2Cu3O7
peut ętre vu comme une pérovskite déficitaire en oxygčne 2 types de site pour Cu ( liées essentiellement par sommet ŕ d'autres pyramides ŕ base carrée CuO4) Chaînes de plans carrés CuO4 liés par sommets |
 |
| On peut le constater sur la représentation polyédrale | 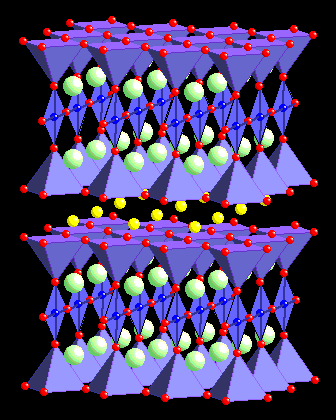 |
Approche topologique des structures - Réseaux
Concept de CONNECTIVITE (P) d'un réseau liant des unités structurales (atomes ou groupes)
Structures des élements non-métalliques, P = 8 - N
P = 1 - I2 - DIMERES
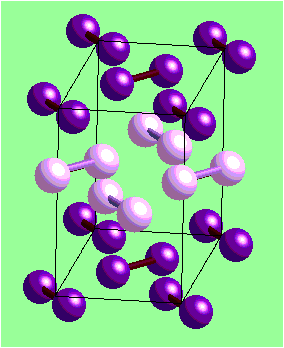 |
L'Iode tend
vers un état metallique (cfc) ŕ haute pression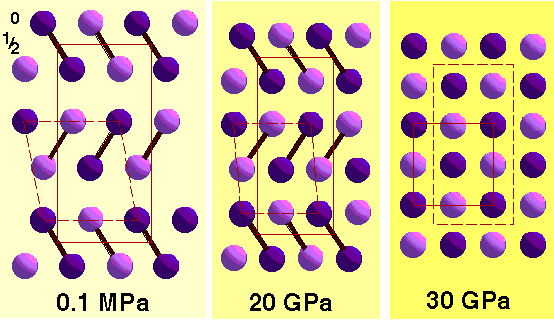
|
P = 2 - S8 CYCLES
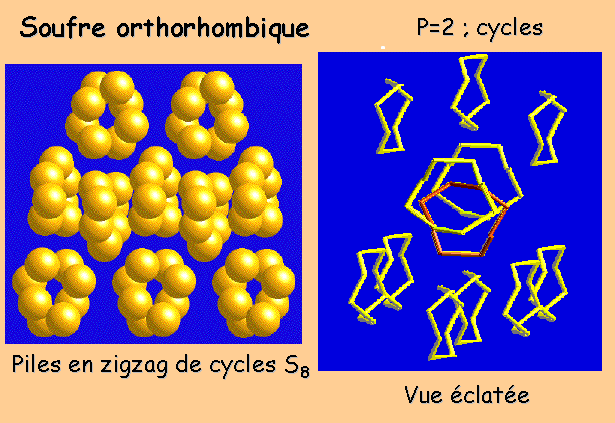
Noter que l'empilement se rapproche d'un arrangement compact |
P = 2 - α-Se CHAINES
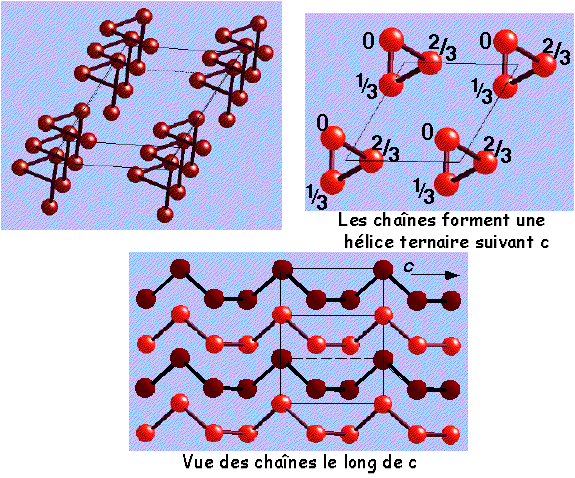 |
P = 3 - COUCHES : As
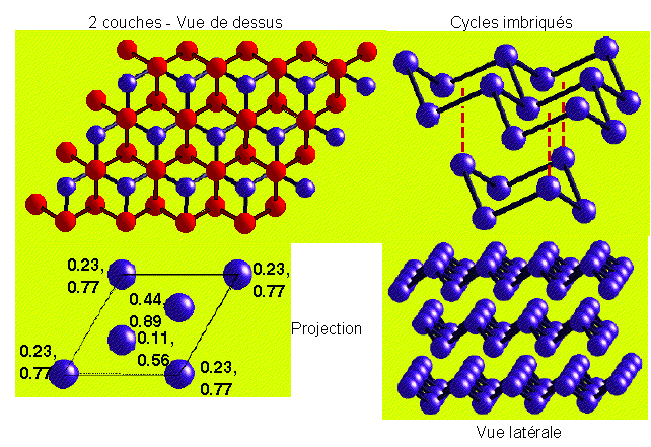 |
Allotropie du CARBONEp avec P = 3
Le carbone montre aussi bien des réseaux en couche ou en cage avec P=3
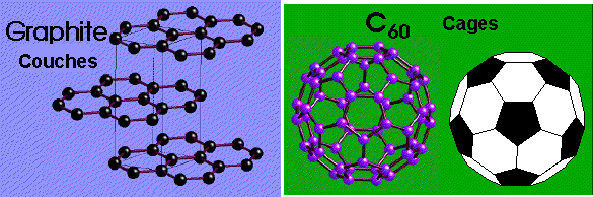
Le réseau Carbone diamant avec P = 4
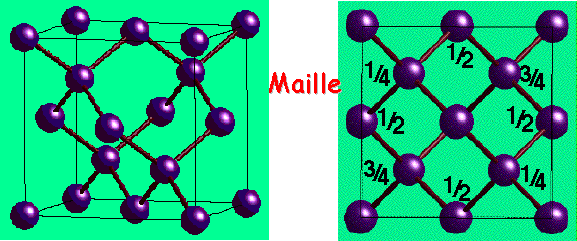

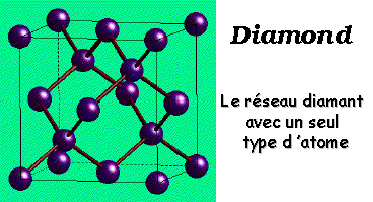
Structures possčdant le réseau Diamant
Réseaux P = 4

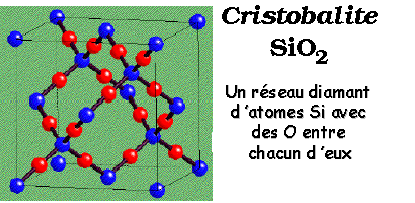
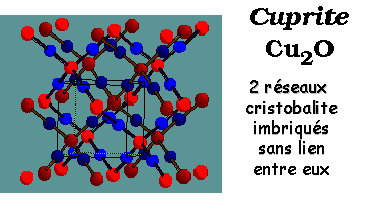
| La
structure Cuprite - un type de réseau intéressant |
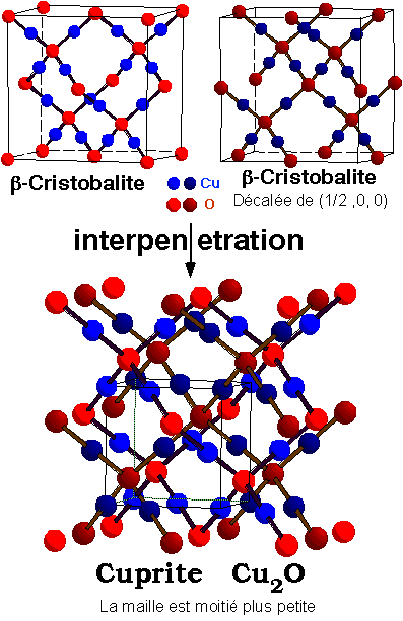 |
Silicates minéraux - Les réseaux de tétračdres SiO44-

| |
Lecture 1 - Lecture 2 - Lecture 3 |
|
© S.J.Heyes, Oxford, 1996 Traduction -Adaptation: Pr C. Jacoboni, Université du Maine, 1998